
Autor:
Křemík
Základní charakteristika
- chemická značka Si
- protonové číslo 14
- má vlastnosti nekovů, je polovodič → bere se jako polokov
- 14. skupina (IV.A)
- elektronová konfigurace 14Si 10[Ne] 3s2 3p2
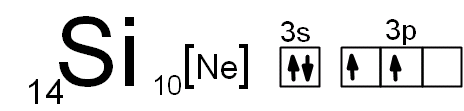
- nachází se ve sloučeninách s kyslíkem v různých minerálech
- má strukturu podobnou diamantu (tvoří kovalentní krystaly)
- málo reaktivní, tvrdý, křehký
- používá se pro výrobu tranzistorů, solárních článků, integrovaných obvodů
- musí být velmi čistý!!
- zákon 10N … 99,99999999 %
- Výroba křemíku: čistý křemík se získá redukcí koksem
-
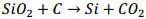
- Výskyt: křemen, křemičitany, hlinitokřemičitany
Sloučeniny křemíku
1. Bezkyslíkaté
Silany
- formálně podobné alkanům, obecný vzorec – SinH2n+2
- SiH4 – monosilan; Si2H6 – disilan; …; Si8H18 – oktasilan
- nestálé
- na vzduchu se samovolně zapalují nebo explodují
SiC – karbid křemíku
- Výroba: reakcí uhlíku s oxidem křemičitým za vysoké teploty (2000°C-2500°C)
-
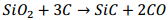
- tepelně stálý, velmi tvrdý
- používá se na brusný materiál
2. Kyslíkaté sloučeniny křemíku
- Stavebním základem všech kyslíkatých sloučenin křemíku je křemíko-kyslíkový čtyřstěn → zajišťuje pevnost a stálost
SiO2 – oxid křemičitý (křemen)
- jsou to různě zbarvené odrůdy křemene:
- Ametyst (fialový)
- Opál (bezbarvý, bílý, nažloutlý, oranžově červený, zelený)
- Citrín (žlutá)
- Záhněda (hnědá)
- Křišťál (bezbarvý)
- odolný, pevný materiál
- chemická podstata skla – vyrábí se z SiO2
- Využití: silikagel – slouží k vysoušení
H2SiO3 – kyselina křemičitá
- Vzniká sloučením oxidu křemičitého a různým počtem hydrátů
![]()
SiO32- - křemičitany
- Většinou jsou ve vodě nerozpustné kromě alkalických křemičitanů
- Vodný roztok alkalických křemičitanů se nazývá vodní sklo
- Využití vodního skla: impregnace, k lepení
![]()
Sklo
- Výroba:
-
Tavení sklářského kmene
Sklářský kmen – sloučenina SiO2, Na2CO3 (CaCO3), můžou tam být i kousky starého skla - Potom se buď fouká (nejdražší) nebo se odlije do formy
- Chladí se
- Druhy skel:
- ploché (tabulové)
- křišťálové
- užitkové
- obalové
- optické
- světlované kabely
- plexisklo
pevné = sklo x sklovina = roztavené sklo

Poslat nový komentář